화학 1 분자 구조 극성, 무극성 분자 단원 공부하고 있는데요, 앞에 까지 그냥 모양
[설명]
1. 무극성 분자랑 극성 분자를 구분하는 방범을 잘 모르겠어요
[1] 중심원자 파악이 가장 중요합니다.
(1) 2원자 분자
A2형 분자 = 두 원자가 같은 종류이므로 무조건 무극성 공유결합입니다.
AB 형 분자 = 두 원자가 다른 종류이므로 무조건 극성 공유결합입니다.
(2) 3원자 분자 : AB2 형 분자 = A가 중심원자
A : 비공유 전자쌍이 없을때 : 일자형 = 원자사이는 극성, 분자 전체도 무극성 분자
(분자는 대칭형) 예 BeCl2
A : 비공유 전자쌍이 있을때 : 굽은형 = 원자사이는 극성, 분자 전체도 극성 분자
(분자는 비대칭형) 예 H2O
(3) 4원자 분자 : AB3 형 분자 = A가 중심원자
A : 비공유 전자쌍이 없을때 : 평면삼각형 = 원자사이는 극성, 분자 전체도 무극성 분자
(분자는 대칭형) 예 BH3
A : 비공유 전자쌍이 있을때 : 피라밑형 = 원자사이는 극성, 분자 전체도 극성 분자
(분자는 비대칭형) 예 NH3
(4) 5원자 분자 : AB4 형 분자 = A가 중심원자
A : 비공유 전자쌍이 없음 : 사면체형 = 원자사이는 극성, 분자 전체도 무극성 분자
(분자는 대칭형) 예 CH4, CCl4
* 그러므로 대칭분자 = 무극성, 비대칭 = 극성 분자
중심원자에 비공유 전자쌍이 없으면 대칭= 무극성 분자, 있으면 비대칭 = 극성 분자
(5) 3.4.5 원자 분자에서 3가지 이상 원자로 된 분자
분자는 쌍극자 모멘트를 게산 해서 0이면 무극성, 아니면 극성 분자임
예] AB3C 형 분자 : AB3C 형 분자 = A가 중심원자
A : 비공유 전자쌍이 없음 : 사면체형 = A-B 극성, A-C 극성이고
극성 분자(분자는 비대칭형이나 극성 분자) 예 CH3Cl
2. 대칭일 때 무극성 분자라고 하던데 루이스 구조식에서 대칭을 보면 안 되는 건가요?
무조건 분자 구조를 머릿속으로 생각을 해서 판단해야하나요?
[1] 루이스 구조식에서 대칭을 보면 가장 정확합니다.
[2] 그런데 루이스 구조식이 보기보다 어려워 위 1 의 설명을 참조하면 편합니다.
-
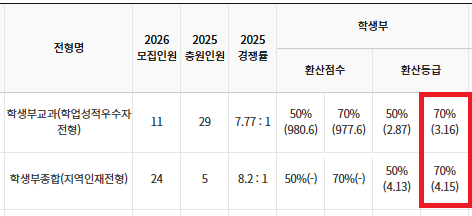
창원대 수시 .. 창원대를 목표로 하고 있는 09년생입니다 지금 제 내신이 5등급제 기준으로
2025.12.01 -
목포에서 롯데월드 가는 법 목포 버스 터미널에서 롯데월드로 갈 수 있는 경로 알려주세요
2025.12.01 -
애니?리뷰 유튜버 찾아주세요ㅠㅠ 무슨 검정머리 남자 캐릭터에 더빙하신분도 남자였던거같은데기승전결로 나눠서 기. 하고 설명하고
2025.12.01 -

발로란트 제한뜨는데 어떻게 해야하나요? 친구가 발로란트 한번해보자고 계정 빌려줬는데 제한이라고 접속이 안되는데 어떻게 해야하나요?
2025.12.01 -

KTX 12월31일 예매 수원이나 서울에서 부산으로 가는 열차를 예매하려고 하는데 언제 열리나요 오늘
2025.12.01 -

한국 지금 쉬었음청년40만명이라는데 4년대학졸업생이 많다던데요 쉬었음청년이 40만명인데 문제가 무엇인가요?
2025.12.01